Spis treści
Czym są onkogeny?
Onkogen to gen komórkowy, którego ekspresja może sprzyjać rozwojowi raka. Jakie są rodzaje onkogenów? Jakimi mechanizmami są aktywowane? Wyjaśnienia.
Co to jest onkogen?
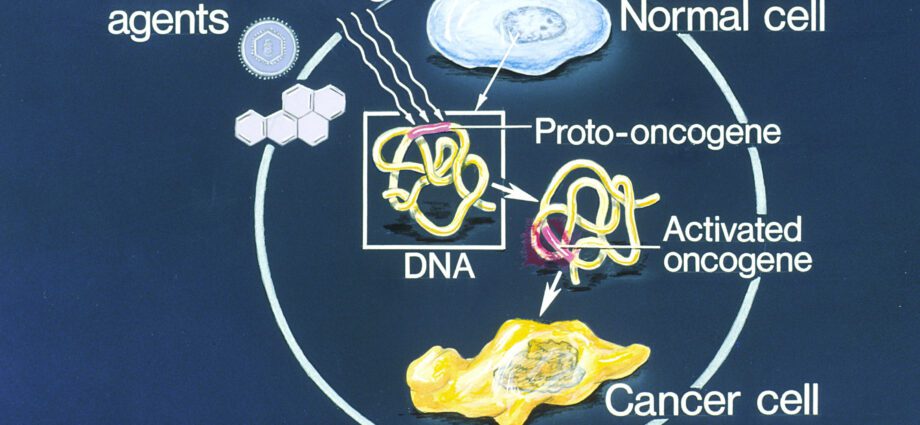
Onkogen (z greckiego onkos, guz i genos, narodziny) zwany także protoonkogenem (c-onc) to gen, którego ekspresja prawdopodobnie nadaje fenotyp rakowy normalnej komórce eukariotycznej. Rzeczywiście, onkogeny kontrolują syntezę białek stymulujących podział komórek (zwanych onkoproteinami) lub hamują zaprogramowaną śmierć komórki (lub apoptozę). Onkogeny są odpowiedzialne za niekontrolowaną proliferację komórek predysponującą do rozwoju komórek nowotworowych.
Onkogeny dzielą się na 6 klas, które odpowiadają odpowiednio kodowanym przez nie onkoproteinom:
- czynniki wzrostowe. Przykład: białka kodujące protoonkogen z rodziny FGF (czynnik wzrostu fibroblastów);
- receptory transbłonowego czynnika wzrostu. Przykład: protoonkogen erb B, który koduje receptor EGF (Epidermal Growth Factor);
- Białka G lub białka błonowe wiążące GTP. Przykład: protoonkogeny z rodziny ras;
- błonowe kinazy tyrozynowe białkowe;
- kinazy białkowe błonowe;
- białka o aktywności jądrowej.Przykład: protoonkogeny Erb A, fos, czerwiec et c-myc.
Jaka jest rola onkogenów?
Odnowę komórkową zapewnia cykl komórkowy. Ta ostatnia jest zdefiniowana przez zestaw zdarzeń, które generują dwie komórki potomne z komórki macierzystej. Rozmawiamy o podział komórek lub „mitoza”.
Cykl komórkowy musi być regulowany. Rzeczywiście, jeśli podział komórek nie jest wystarczający, organizm nie działa optymalnie; I odwrotnie, jeśli podział komórek jest obfity, komórki proliferują w sposób niekontrolowany, co sprzyja pojawianiu się komórek rakowych.
Regulację cyklu komórkowego zapewniają geny podzielone na dwie kategorie:
- antyonkogeny, które hamują proliferację komórek poprzez spowalnianie cyklu komórkowego;
- protoonkogeny (c-onc) lub onkogeny, które promują proliferację komórek poprzez aktywację cyklu komórkowego.
Jeśli porównamy cykl komórkowy do samochodu, antyonkogeny będą hamulcami, a protoonkogeny akceleratorami tych ostatnich.
Anomalie, patologie związane z onkogenami
Wygląd guza może wynikać z mutacji inaktywującej antyonkogeny lub przeciwnie, z mutacji aktywującej protoonkogeny (lub onkogeny).
Utrata funkcji antyonkogenów uniemożliwia im działanie hamujące proliferację komórek. Zahamowanie antyonkogenów otwiera drzwi do niekontrolowanego podziału komórek, który może prowadzić do pojawienia się komórek nowotworowych.
Jednak antyonkogeny są genami komórkowymi, to znaczy występują w duplikacie na parze chromosomów, które niosą je w jądrze komórki. Tak więc, gdy jedna kopia antyonkogenu nie jest funkcjonalna, druga umożliwia działanie jako hamulec tak, że osobnik jest chroniony przed proliferacją komórek i przed ryzykiem nowotworów. Tak jest na przykład w przypadku genu BRCA1, którego mutacja hamująca eksponuje raka piersi. Ale jeśli druga kopia tego genu jest funkcjonalna, pacjent pozostaje chroniony, chociaż jest predysponowany z powodu wadliwej pierwszej kopii. W ramach takiej predyspozycji czasami rozważana jest profilaktyczna podwójna mastektomia.
Odwrotnie, mutacja aktywująca wpływająca na protoonkogeny podkreśla ich stymulujący wpływ na proliferację komórek. Ta anarchiczna proliferacja komórek predysponuje do rozwoju nowotworów.
Podobnie jak antyonkogeny, proonkogeny są genami komórkowymi, występującymi w dwóch powtórzeniach w parze chromosomów, które je niosą. Jednak w przeciwieństwie do antyonkongenów obecność pojedynczego zmutowanego proonkogenu wystarcza do wywołania przerażających efektów (w tym przypadku proliferacji komórek). Pacjent niosący tę mutację jest zatem narażony na ryzyko raka.
Mutacje w onkogenach mogą być spontaniczne, dziedziczne lub nawet wywołane przez mutageny (chemikalia, promienie UV itp.).
Aktywacja onkogenów: zaangażowane mechanizmy
U źródeł aktywujących mutacji onkogenów lub proonkogenów (c-onc) leży kilka mechanizmów:
- integracja wirusa: insercja wirusa DNA na poziomie genu regulatorowego. Tak jest na przykład w przypadku wirusa brodawczaka ludzkiego (HPV), który jest przenoszony drogą płciową;
- mutacja punktowa w sekwencji genu kodującego białko;
- delecja: utrata większego lub mniejszego fragmentu DNA, stanowiącego przyczynę mutacji genetycznej;
- rearanżacja strukturalna: zmiana chromosomalna (translokacja, inwersja) prowadząca do powstania genu hybrydowego kodującego niefunkcjonalne białko;
- amplifikacja: nieprawidłowe zwielokrotnienie liczby kopii genu w komórce. Ta amplifikacja generalnie prowadzi do wzrostu poziomu ekspresji genu;
- deregulacja ekspresji RNA: geny są odłączane od ich normalnego środowiska molekularnego i umieszczane pod nieodpowiednią kontrolą innych sekwencji, powodując modyfikację ich ekspresji.
Przykłady onkogenów
Geny kodujące czynniki wzrostu lub ich receptory:
- PDGF: koduje czynnik wzrostu płytek krwi związany z glejakiem (rakiem mózgu);Erb-B: koduje receptor naskórkowego czynnika wzrostu. Związany z glejakiem (rakiem mózgu) i rakiem piersi;
- Erb-B2 zwany także HER-2 lub neu: koduje receptor czynnika wzrostu. Związany z rakiem piersi, gruczołu ślinowego i jajnika;
- RET: koduje receptor czynnika wzrostu. Związany z rakiem tarczycy.
Geny kodujące przekaźniki cytoplazmatyczne w szlakach stymulacji:
- Ki-ras: związany z rakiem płuc, jajnika, okrężnicy i trzustki;
- N-ras: związane z białaczką.
Geny kodujące czynniki transkrypcyjne, które aktywują geny promujące wzrost:
- C-myc: związany z białaczką i rakiem piersi, żołądka i płuc;
- N-myc: związany z nerwiakiem niedojrzałym (nowotwór komórek nerwowych) i glejakiem;
- L-myc: związany z rakiem płuc.
Geny kodujące inne cząsteczki:
- Hcl-2: koduje białko, które normalnie blokuje samobójstwo komórek. Związany z chłoniakami limfocytów B;
- Bel-1: również nazywany PRAD1. Koduje Cyclin DXNUMX, aktywator zegara cyklu komórkowego. Związany z rakiem piersi, głowy i szyi;
- MDM2: koduje antagonistę białka wytwarzanego przez gen supresorowy guza.
- P53: związany z mięsakami (raki tkanki łącznej) i innymi nowotworami.
Skoncentruj się na wirusach okongenicznych
Wirusy onkogenne to wirusy, które mają zdolność do powodowania rakotwórczych komórek, które infekują. 15% nowotworów ma etiologię wirusową, a te nowotwory wirusowe są przyczyną około 1.5 miliona nowych przypadków rocznie i 900 zgonów rocznie na całym świecie.
Powiązane nowotwory wirusowe są problemem zdrowia publicznego:
- wirus brodawczaka jest związany z prawie 90% raków szyjki macicy;
- 75% wszystkich raków wątroby jest związanych z wirusem zapalenia wątroby typu B i C.
Istnieje pięć kategorii wirusów onkogennych, niezależnie od tego, czy są to wirusy RNA, czy wirusy DNA.
Wirusy RNA
- Retroviridae (HTVL-1) naraża cię na ryzyko wystąpienia białaczki T;
- Flaviviridae (wirus zapalenia wątroby typu C) jest zagrożony rakiem wątrobowokomórkowym.
Wirusy DNA
- Papovaviridae (wirus brodawczaka 16 i 18) naraża na raka szyjki macicy;
- Herpesviridae (wirus Esptein Barr) naraża się na chłoniaka B i raka;
- Herpesviridae (ludzki herpeswirus 8) naraża na chorobę Kaposiego i chłoniaki;
- Hepadnaviridae (wirus zapalenia wątroby typu B) jest podatny na raka wątrobowokomórkowego.